
Na chamada tabela periódica podemos ver os elementos químicos, que são ordenados por seu número atômico, bem como por sua configuração eletrônica, sem esquecer suas propriedades químicas. Tudo isso significa que temos diante de nós um arranjo em forma de mesa.
É por isso que podemos definir a tabela periódica como um tipo de esquema que nos permite entender melhor cada um dos elementos, ao estudar química. Mas há muito mais que hoje você vai descobrir.
O que é a tabela periódica e para que serve?

Com certeza você já sabia que é um esquema, onde aparecem os elementos químicos. Mas não estão ali por acaso, mas a sua colocação e os dados que a dita tabela nos dá, têm um propósito. O objetivo será conhecer as semelhanças e tudo o que difere de cada um dos elementos principais. Tudo isso para poder aplicá-lo de forma prática.
Os elementos são distribuídos da esquerda para a direita e de cima para baixo, mas sempre seguindo a ordem crescente de seus números atômicos, ou seja, número de prótons. As linhas horizontais que a tabela periódica de elementos possui são chamadas de períodos, enquanto as 18 colunas verticais são chamadas de grupos ou famílias.
Desenvolvimento de elementos atômicos, propriedades e pesos
É preciso dizer que alguns dos elementos já eram bem conhecidos na antiguidade. Ouro, prata, bem como cobre ou mercúrio eram os principais. Mas, realmente, a primeira descoberta de um elemento químico ocorreu no século XNUMX. Foi graças a Henning Brand que ele descobriu o fósforo. Já no século XNUMX, outros como o hidrogênio ou o oxigênio tornaram-se conhecidos. Era assim Antoine Lavoisier elaborou uma lista de cerca de 33 itens, que os agrupou em gases, metais, não metais e terra. No início do século XNUMX, foi John Dalton quem desenvolveu uma nova ideia. Tratava-se da formulação de um atomismo químico, construindo assim um sistema de massas atômicas relativas. Embora Dalton preferisse chamá-los de pesos atômicos. Posteriormente, suas ideias também foram modificadas, pois apresentavam algumas imprecisões.
Estrutura da tabela periódica e seus elementos
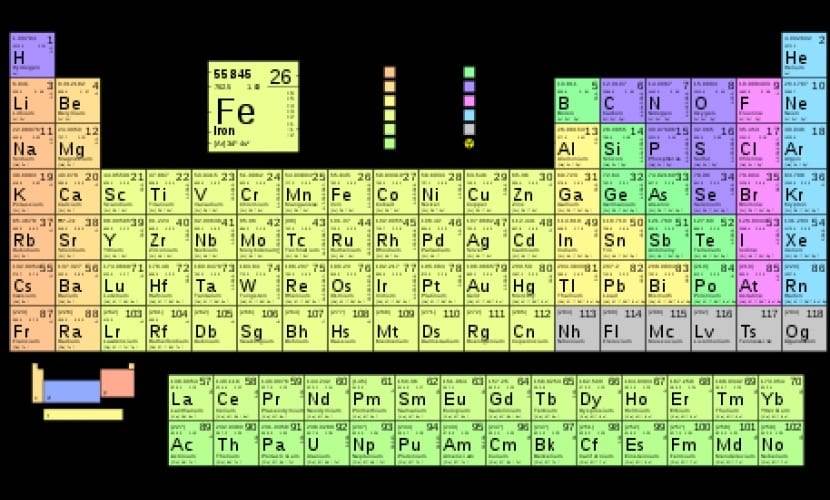
Depois de todos os estudos e avanços, temos um total de 118 elementos. Nós os encontraremos divididos nos chamados grupos ou famílias e os períodos. Quer saber o que cada um simboliza?
Grupos ou famílias
São as colunas verticais que podemos ver na tabela. São um total de 18, na tabela que todos conhecemos hoje e como podemos constatar estão devidamente numerados. Os elementos em cada grupo têm propriedades físicas e químicas muito semelhantes.
- Grupo 1: Nele vamos conhecer o metais alcalinos. É constituído pelos elementos lítio (Li), sódio (Na), potássio (K), rubídio (Rb), césio (Cs), frâncio (Fr).
- Grupo 2: Neste segundo grupo, veremos o metais alcalinos terrestres. Eles são mais difíceis do que os anteriores e bons condutores elétricos. Aqui encontraremos berílio (Be), magnésio (Mg), cálcio (Ca), estrôncio (Sr), bário (Ba) e rádio (ra).
- Grupo 3: Família Escandio. Entre eles estão o escândio (Sc) e o ítrio (Y). Embora sejam um tanto contestados, o lantânio (La) e o actínio (Ac) também devem ser mencionados.
- Grupo 4Es o família do titânio. Nele encontramos titânio (ti), zircônio (Zr), háfnio (Hf) e rutherfórdio (Rf).
- Grupo 5: Dentro da família vanádio, vamos encontrar vanádio (V), nióbio (Nb), tântalo (Ta), dubnium (Db).
- Grupo 6: Neste grupo encontramos o família cromo. Lá veremos cromo (Cr), molibdênio (Mo), tungstênio (W), seabórgio (Sg).
- Grupo 7: manganês (Mn), tecnécio (Tc) e rênio (Re), todos pertencentes à família do manganês.
- Grupo 8: A família de ferro É composto de ferro (Fe), rutênio (Ru), ósmio (Os), Hassium (Hs).
- Grupo 9: Aqui encontramos cobalto (Co), ródio (Rh), Iridium (Ir), meitnerium (Mt).
- Grupo 10: A família do níquel é composta por níquel (Ni), paládio (Pd), platina (Pt), darmstádio (Ds).
- Grupo 11: Cobre (Cu), prata (Ag) e ouro (Au) são conhecidos como cunhagem de metais, embora não seja um termo que todos aceitem.
- Grupo 12: Zinco (Zn), cádmio (Cd) e mercúrio (Hg).
- Grupo 13: O denominado grupo 13 também corresponde ao grupo do boro. Um nome que vem da terra, porque é onde eles são mais abundantes. Encontramos boro (B), alumínio (Al), gálio (Ga), índio (In), tálio (Ti) e niônio (nh).
- Grupo 14: No carbono ou grupo carboneto, encontramos carbono (C), silício (Si), germânio (Ge), estanho (Sn), chumbo (Pb), phlerovium (FI).
- Grupo 15: Neste caso, chegamos a grupo nitrogênio. Claro, começamos com nitrogênio (N), fósforo (P), arsênio (As), antimônio (Sb), bismuto (Bi) e muscovio (Mc).
- Grupo 16: É conhecido como o grupo dos Anfígenos, embora eles não possam esconder seu status de família do oxigênio. Assim, encontramos oxigênio (O), enxofre (S), selênio (Se), telúrio (Te), polônio (Po), livermorio (Lv).
- Grupo 17: O halogênios estão neste grupo. Flúor (F), Cloro (CI), Bromo (Br), Iodo (I), Astato (At), Tenese (Ts).
- Grupo 18: As chamadas gases nobres Eles são outro dos grupos de elementos que possuem propriedades muito semelhantes. Em condições normais, são considerados gases incolores e inodoros. Os gases são hélio (He), néon (Ne), argônio (Ar), criptônio (Kr), xenônio (Xe), radônio (Rn) e organéson (Og).
Para entender esta organização, você tem que saber que cada um dos membros de um grupo tem características muito semelhantes como sua configuração eletrônica e a mesma valência, ou seja, o número de elétrons que possuem na última camada. Claro, quando olhamos de cima para baixo e no mesmo grupo, veremos como os raios atômicos de cada um dos elementos que o compõem aumentam.
Períodos
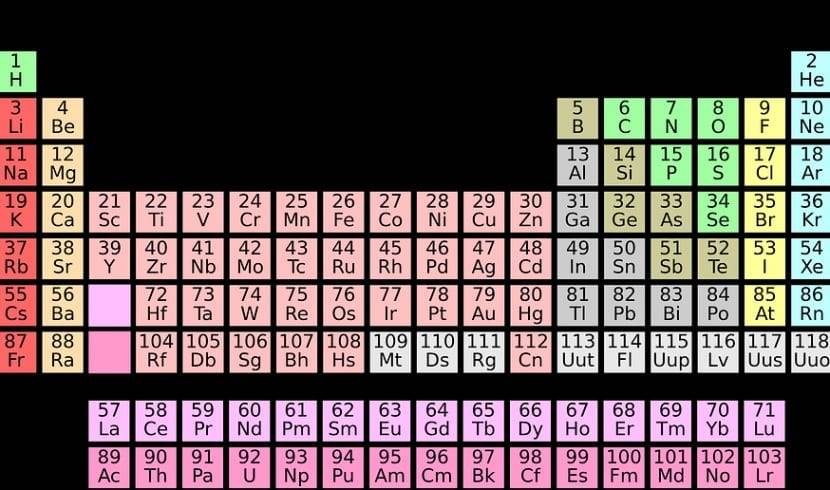
Se agora nos concentrarmos no linhas horizontais que compõem a tabela periódica, então nos leva a falar sobre os períodos. Dependendo de qual período cada elemento pertence, ele indicará o número de níveis de energia de um átomo. Eles são organizados por níveis e subníveis, mas sempre, os elementos continuarão a ser organizados de acordo com seu número atômico.
- Período 1: No período um, temos apenas dois elementos químicos. Hidrogênio e hélio.
- Período 2: Neste caso, o número atômico aumenta um pouco mais e vamos encontrar um total de oito elementos, entre os quais lítio, boro, carbono ou nitrogênio, entre outros, como vemos na imagem.
- Período 3: Sódio, Magnésio, Alumínio, Silício, Fósforo ou Enxofre, encontram-se neste período.
- Período 4: A quarta linha da tabela periódica já contém mais elementos. Um total de 18 serão os que nele estiverem localizados. Podemos citar potássio e cálcio ou ferro e zinco.
- Período 5: Bem, como já sabemos, corresponde à quinta linha da tabela de elementos. Ele também tem um total de 18. Aqui encontraremos estrôncio ou paládio.
- Período 6: Outros 18 elementos estão na chamada sexta linha ou período 6. Alguns deles são césio, tungstênio ou mercúrio.
- Período 7: Os elementos mais radioativos e instáveis são encontrados neste período 7. Actinídeos também estão incluídos.
Divisão de blocos

Para realizar a divisão da tabela de elementos do bloco, leva-se em consideração o orbital no qual reside o último elétron.
- Bloco s: O bloco s corresponde aos dois primeiros grupos, ou seja, os grupos alcalino e alcalino-terroso, sem esquecer o hélio e o hidrogênio.
- Bloco p: Corresponde aos últimos seis grupos. Contém todos os metalóides.
- Bloco d: Os grupos 3 a 12 estariam neste bloco. Você pode dizer que os metais de transição estão nele.
- Bloco f: É constituído por lantanídeos e actinídeos.
Qual é a importância da tabela de elementos?
Como vimos, a tabela mostra-nos e apresenta os elementos de forma simples. Por um lado, encontramos os elementos, propriamente falando, representados por um símbolo. Na tabela mais comum, podemos ver como apenas duas figuras o acompanham. Um deles se referirá ao seu número de massa, ou seja, a soma de prótons e nêutrons. Por outro lado, o número atômico (número de prótons), geralmente é colocado como um subscrito e à esquerda do elemento. Com tudo isso, a mesa é uma ferramenta perfeita para nosso aprendizado.
Como usar a tabela periódica

Para muitos, segurar a tabela periódica é mais do que um hieróglifo. É por isso que todas as suas divisões, números e até cores têm um significado. Você tem que saber o que cada uma dessas seções lhe diz:
- Símbolos: O símbolo é o representação de elemento. Possui uma letra maiúscula e às vezes é acompanhada por outras letras minúsculas, dependendo do caso.
- classificação: Como vimos anteriormente, a classificação ou grupos onde cada um dos elementos aparece também é importante.
- Número atômico: Cada átomo possui um número atômico. Isso é igual a número de prótons em seu núcleo. Este número diferencia um elemento do outro. Geralmente é colocado antes do próprio elemento. Por exemplo, o boro (B) tem o número 5. Este é o seu número atômico. Possui 5 elétrons ao redor do núcleo e 5 prótons em seu núcleo.
- Massa atômica: É a massa do átomo e é expressa em unidades (amu).
- Número de prótons: O número de prótons de qualquer átomo é igual ao seu número atômico.
- Número de nêutrons: Igual a massa atômica menos o número de prótons.
- Cor dos elementos: Indica seu reflexo da luz quando falamos sobre condições normais.
- Volume atômico: É definido como o volume ocupado por um mole de átomos de um elemento.
Novos elementos químicos na tabela
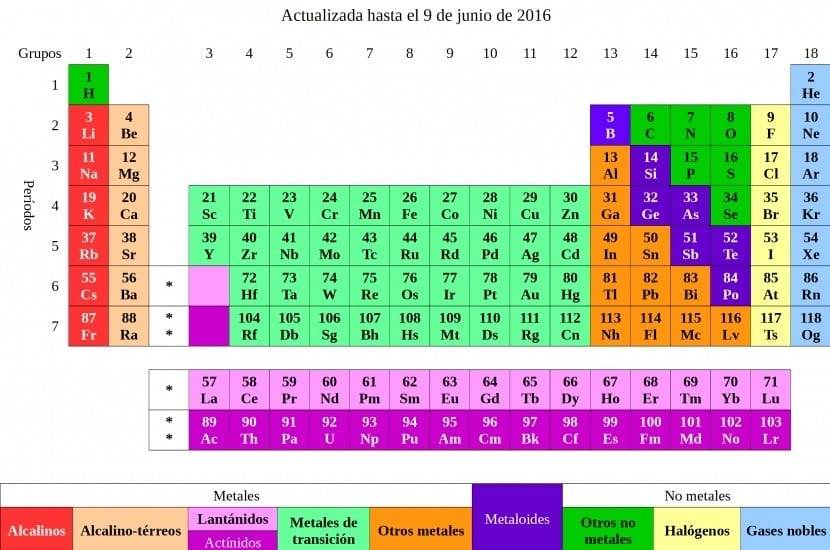
Parece que quando aprendemos a tabela periódica usual, alguns novos elementos aparecem. Especificamente, eles estão localizados na sétima linha e há quatro que você precisa saber. Eles são nomeados após: Moscovio, Teneso, Nihonium e Oganesón. É preciso dizer que o elemento Nihonium foi descoberto por alguns cientistas japoneses e os outros estão divididos entre a Rússia e os Estados Unidos.